
- English
- Español
- Português
- русский
- Français
- 日本語
- Deutsch
- tiếng Việt
- Italiano
- Nederlands
- ภาษาไทย
- Polski
- 한국어
- Svenska
- magyar
- Malay
- বাংলা ভাষার
- Dansk
- Suomi
- हिन्दी
- Pilipino
- Türkçe
- Gaeilge
- العربية
- Indonesia
- Norsk
- تمل
- český
- ελληνικά
- український
- Javanese
- فارسی
- தமிழ்
- తెలుగు
- नेपाली
- Burmese
- български
- ລາວ
- Latine
- Қазақша
- Euskal
- Azərbaycan
- Slovenský jazyk
- Македонски
- Lietuvos
- Eesti Keel
- Română
- Slovenski
- मराठी
- Srpski језик
Bosutinib CAS 380843-75-4
2023-08-21
Nombre químico:
4-(2,4-dicloro-5-metoxianilino)-6-metoxi-7-[3-(4-metilpiperazin-1-il)propoxi]quinolin-3-carbonitrilo
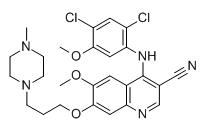
MF:C26H29Cl2N5O3
Propiedades químicas :Amarillo pálido sólido
Bosutinib es un inhibidor de la quinasa Bcr-Abl para el tratamiento de la leucemia mielógena crónica (LMC) con cromosoma Filadelfia positivo (Ph+). En comparación con otros inhibidores de la tirosina quinasa, tiene un perfil de toxicidad hematológica más favorable. Aprobado por la FDA el 4 de septiembre de 2012.
Innovador:Wyeth Pharmaceuticals (Pfizer) (EE. UU.)
Aplicaciones:
Se observaron efectos sobre la morfología celular a una concentración de SKI-606 1 µM para todas las líneas celulares examinadas, y los cambios morfológicos fueron evidentes a concentraciones tan bajas como 0,25 µM. SKI-606 hizo que las células se adhirieran entre sí, formando grupos densos en comparación con las células tratadas con control de vehículo (DMSO), que mostraron diseminación en áreas más grandes.
Forma farmacéutica: Administración oral, 100 mg/Kg/d, durante 28 días.
Intermedios:
No. CAS 2031-23-4 diclorhidrato de 1-(3-cloropropil)-4-metilpiperazina
No. CAS 214470-66-3 7-(3-cloropropoxi)-4-hidroxi-6-metoxiquinolina-3-carbonitrilo
No. CAS 214470-68-5 4-CLORO-7-(3-CLORO-PROPOXI)-6-METOXI-QUINOLINA-3-CARBONITRILO
No. CAS 263149-10-6 4-CLORO-7-HIDROXI-6-METOXI-QUINOLINA-3-CARBONITRILO
No. CAS 380844-49-5 7-(3-CLORO-PROPOXI)-4-(2,4-DICLORO-5-METOXI-FENILAMINO)-6-METOXI-QUINOLINA-3-CARBONITRILO
El fármaco dirigido Bsutinib (Bosulif) ha sido aprobado por la Administración de Alimentos y Medicamentos (FDA) para el tratamiento de la leucemia mielógena crónica. Besutinib es un inhibidor de la quinasa que inhibe las vías de señalización Abl y Src. El medicamento está destinado a tratar pacientes adultos con leucemia mieloide crónica crónica, acelerada o aguda con cromosoma Filadelfia positivo (Ph+) con resistencia o intolerancia previa a los medicamentos, según un anuncio de Pfizer Oncology. Alrededor de un tercio de los pacientes con leucemia mieloide crónica no responden bien al tratamiento con el fármaco estándar de primera línea Gleevec, afirmó Pfizer. Aproximadamente la mitad de los pacientes que desarrollan resistencia o intolerancia al imatinib también responden mal a otros inhibidores de la tirosina quinasa (TKI) de segunda línea, dijo la compañía.
La aprobación del fármaco oral se basó principalmente en ensayos clínicos de fase I y fase II en los que participaron 500 pacientes con leucemia mieloide crónica con PH positivo que no respondían o eran intolerantes al imatinib, incluidos diferentes grupos en las etapas crónica, acelerada y aguda. Según los datos del ensayo clínico de Pfizer, un tercio de los pacientes tratados previamente con imatinib solo lograron una remisión citogenética importante después de 24 semanas de tomar bosutinib (500 mg una vez al día). En los pacientes que recibieron imatinib y otro inhibidor de la tirosina quinasa (dasatinib, Sprycel), el 27 % logró una remisión citogenética importante. Las tasas de respuesta continuaron aumentando en ambos grupos después de 24 semanas o más de tomar el medicamento, dijo Pfizer. Pfizer señala que sólo el 4 por ciento de los pacientes con enfermedades crónicas progresan a la etapa avanzada o aguda después de tomar Besutinib. Los efectos secundarios de grado 3-4 incluyen trombocitopenia (26%), neutropenia (11%), diarrea (9%), anemia (9%) y erupción cutánea (8%).
Bosutris (Bosutinib) bossutinib fue desarrollado originalmente por Pfizer y fue aprobado por primera vez en los Estados Unidos en septiembre de 2012 para su uso en adultos con LMC Ph+ que han tenido antecedentes de resistencia o intolerancia al tratamiento en etapas crónica, acelerada o aguda. . BOSULIF es el primer fármaco de Pfizer para tratar tumores hematológicos y es una opción de tratamiento importante para pacientes con leucemia mieloide crónica Ph+ con intolerancia o resistencia previa a los medicamentos. Esta indicación ampliada tiene el potencial de tener un impacto aún mayor en las vidas de los pacientes con leucemia mielógena crónica.
El 13 de julio de 2020, Mylan Pharmaceutical de la India abrió el lanzamiento comercial de Bosutinib (Bosutinib/Bosutinib/Bosutinib) genérico Bosutris. Una versión genérica de Bosutris de Mylan cuesta alrededor de un 25% menos que el Bosulif original de Pfizer. (Además: Upjohn, la división de genéricos de Pfizer, se fusionará con Mylan este año para crear Viatris, la empresa de genéricos más grande del mundo, que se completará en el cuarto trimestre de 2020).




